Mitocondrias y cáncer: explorando la maquinaria interna de la enfermedad
Diana Lashidua Fernández Coto y Marisol Ayala Reyes
De una completa extraña a una socia inseparable: el origen de la mitocondria
Las mitocondrias son componentes de las células que conforman el cuerpo humano. Pero, ¿sabías que las mitocondrias no siempre fueron parte de nuestras células? Según una teoría propuesta por Lynn Margulis, las mitocondrias surgieron como un tipo especial de bacteria que se integró en una célula huésped. La bacteria se convirtió en lo que hoy conocemos como mitocondria. Esta teoría es ampliamente aceptada pues la similitud entre las bacterias y la mitocondria es indiscutible: posee una doble membrana y su propio material genético, conocido como ADN mitocondrial (ADNmt), que es diferente al ADN que se encuentra en el núcleo de nuestras células.
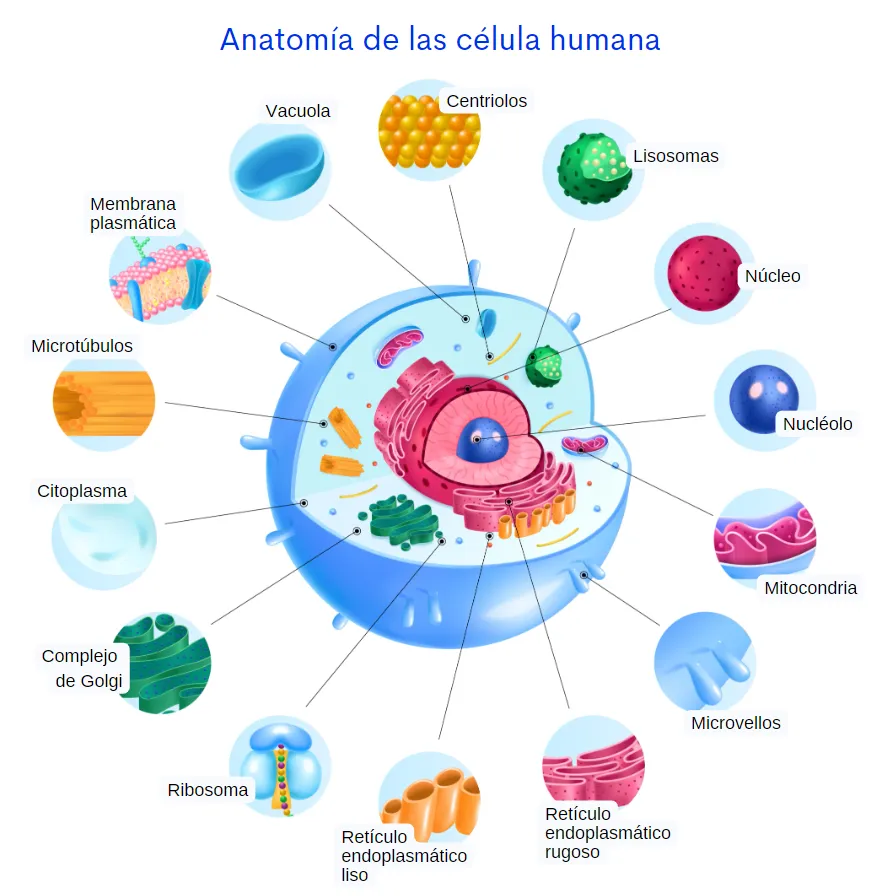
La figura 1 muestra como se ve una mitocondria y destaca su estructura de doble membrana y el ADNmt.

Figura 1. Estructura y localización de la mitocondria en la célula. La célula contiene varias mitocondrias localizadas en el citoplasma celular. Cada una posee una membrana externa lisa y una membrana interna plegada (crestas) separadas por el espacio intermembranal. Contiene su propio ADN (ADNmt) y ribosomas para producir proteínas importantes para procesos mitocondriales como la generación de energía (Imagen creada por las autoras en BioRender).
El éxito en la integración de una bacteria como componente permanente de una célula se dio gracias al beneficio mutuo. La célula huésped ofrecía un ambiente abundante en nutrientes. Mientras que la mitocondria, tenía la capacidad de proporcionar la energía necesaria para la célula. A su vez surgió una cooperación entre ambos tipos de material genético (nuclear y mitocondrial), implicando la transferencia y el origen de nuevos genes, así como la integración de ambos metabolismos.
La manera en que las mitocondrias generan energía para las células es a través de la respiración celular. La mitocondria utiliza diversas vías metabólicas para producir moléculas energéticas, dentro de las cuales destaca el trifosfato de adenosina (ATP). Cuando una célula requiere energía, escinde uno de los tres fosfatos del ATP, convirtiéndolo en ADP (difosfato de adenosina). Esta ruptura del fosfato libera energía que la célula utiliza principalmente para procesos metabólicos.
Durante la producción de energía, se generan especies reactivas de oxígeno (ROS) también conocidos como radicales libres, que son moléculas inestables que tienden a reaccionar fácilmente con otras moléculas en la célula. La producción controlada de estas especies permite el correcto funcionamiento en la célula, no obstante, su aumento causa daños importantes tanto en las mitocondrias como en la célula.
Estos daños en las mitocondrias afectan su funcionamiento en la respiración celular y en otros procesos en los que participan relacionados con el crecimiento, división y muerte celular. Además, estas alteraciones pueden contribuir al desarrollo de diversas enfermedades humanas, como enfermedades cardiovasculares, neurodegenerativas, algunos tipos de diabetes y, de manera importante, el cáncer.
Alteraciones del metabolismo mitocondrial en el cáncer
En el citoplasma de las células normales, los productos generados en la glucólisis (el proceso por el que se descompone una molécula de glucosa), ingresan a la mitocondria para ser utilizados en la generación de energía a través de lo que se conoce como la cadena de transporte de electrones (CTE) y el sistema de la fosforilación oxidativa (OXPHOS). La CTE se compone por complejos formados por la asociación de varias proteínas unidos a la membrana interna mitocondrial (Figura 1). Estos complejos trabajan en conjunto para llevar a cabo la respiración celular dependiente de oxígeno, lo que finalmente permite que la enzima llamada “ATP sintetasa” produzca de 24 a 28 moléculas energéticas de ATP.
En las células cancerosas, se observa una alteración en las vías metabólicas utilizadas para la generación de energía, lo cual puede ser resultado de mutaciones (cambios en la secuencia) en el ADNmt u otros mecanismos. En este caso, los productos de la glucólisis no ingresan a la mitocondria y se generan solo dos moléculas de ATP. A este fenómeno que solo ocurre en células cancerosas se le conoce como reprogramación metabólica o “efecto Warburg”, ya que fue descrito por primera vez por el fisiólogo alemán Otto Warburg.
Se podría pensar que la división de las células cancerosas se vería limitada por la ineficiente producción de ATP a través de la glucólisis, ya que solo se producen dos moléculas de ATP por cada molécula de glucosa; no obstante, se ha observado que la glucólisis es aproximadamente 100 veces más rápida que la respiración celular dependiente de oxígeno. Como resultado, el crecimiento y división de las células cancerosas es muy acelerado. Además, a pesar del mal funcionamiento de las mitocondrias y en consecuencia el aumento de radicales libres en la célula, las células cancerosas tienen la capacidad de adaptar su metabolismo y continuar con su ciclo de crecimiento.
Normalmente, cuando una célula cumple su ciclo de vida o sufre algún daño que perjudica su función, el sistema inmune se encarga de eliminarla, sin embargo, la reprogramación metabólica les da a las células cancerosas la habilidad para escapar de este ataque. Asimismo, les confiere la habilidad de resistencia a los tratamientos más comúnmente utilizados en cáncer como la quimioterapia y la radioterapia.
Otros procesos regulados por las mitocondrias que se han visto alterados en las células tumorales son: 1) la mitofagia, un proceso mediante el cual las células degradan y eliminan las mitocondrias dañadas; 2) la apoptosis intrínseca, también conocida como muerte celular programada que ocurre como respuesta a señales internas de estrés o daño celular; y 3) la biogénesis mitocondrial, en donde las células producen nuevas mitocondrias como respuesta al estrés metabólico; entre otros (Figura 2).

Figura 2. Alteración de los procesos mitocondriales que favorecen la reprogramación metabólica característica de células tumorales (Imagen creada por las autoras en BioRender).
¿Cómo estudiamos las mitocondrias?
Actualmente se tiene un particular interés en aclarar la importancia de las mitocondrias en enfermedades como el cáncer. En el laboratorio de proteómica del Centro de Ciencias Genómicas de la UNAM, liderado por el Dr. Sergio Encarnación Guevara, hemos desarrollado una técnica para obtener un extracto enriquecido de mitocondrias. Las herramientas con las que contamos en el laboratorio nos han permitido indagar en lo que se llama “el proteoma mitocondrial”, es decir, todas las proteínas que poseen las mitocondrias, y hemos identificado las diferencias entre las proteínas producidas en células cancerosas y en células no cancerosas.
Además, hemos llevado a cabo estudios sobre modificaciones en proteínas mitocondriales. Sabemos que la función, estructura y localización de las proteínas mitocondriales se regula gracias a pequeñas moléculas que se unen a sus aminoácidos y la modifican. En la acetilación, por ejemplo, la molécula de acetilo (formada por dos átomos de carbono y tres de oxígeno) se une al aminoácido lisina. Se ha visto que esta unión o modificación tiene implicaciones en la reprogramación metabólica de células cancerosas, por lo que ha sido ampliamente estudiada.
De esta manera buscamos ampliar el conocimiento actual que se tiene sobre la regulación de las proteínas mitocondriales en el cáncer, mediante el proceso de acetilación/desacetilación del aminoácido lisina. Nuestro objetivo es contribuir al desarrollo de terapias potenciales y estrategias de diagnóstico en este campo.

Figura 3. Flujo de trabajo para el enriquecimiento y procesamiento de mitocondrias. Se cultivan células sanas y cancerosas, las células se rompen y se enriquecen las mitocondrias a través de centrifugación mediante un gradiente de concentración de sacarosa (aumento gradual de concentraciones de sacarosa) para obtener las proteínas de este componente celular. Estas se analizan por espectrometría de masas (técnica que permite la identificación de proteínas y otras moléculas) para observar posibles proteínas que se producen en las células cancerosas y no en células sanas (marcadores) (Imagen creada por las autoras en BioRender).
En uno de nuestros estudios sobre el cáncer de estómago, que hemos publicado en una revista científica especializada [1], se analizaron muestras de tejido de pacientes en diferentes etapas de la enfermedad. Este estudio reveló la alteración de distintos procesos celulares. Descubrimos que algunas proteínas importantes para el funcionamiento de las mitocondrias disminuyen su producción en el cáncer, y en cambio se observó una mayor actividad en proteínas asociadas al uso de glucosa como fuente de energía, sugiriendo un daño en los procesos mitocondriales para la obtención de energía en células cancerosas de estómago. Además, identificamos varias proteínas que se producen en células cancerosas y no en células sanas que son denominadas marcadores ya que funcionan como indicadores detectables de la enfermedad y ayudan a su diagnóstico.
Actualmente seguimos trabajando con este y otros tipos de cáncer con el objetivo de proporcionar una base sólida para el diagnóstico y el desarrollo de terapias más eficaces y precisas. No obstante, al ser un campo de estudio sumamente amplio, aún nos queda mucho por descubrir sobre las mitocondrias, su funcionamiento y sus implicaciones en la salud.
Referencias
- Fernández-Coto, D., Gil, J., Hernández, A., Herrera-Goepfert, R., Castro-Romero, I., Hernández-Márquez, E., Arenas-Linares, A., Calderon-Sosa, V., Sanchez-Aleman, M., Mendez-Tenorio, A., Encarnación-Guevara, S. y Ayala, G. (2018). Quantitative proteomics reveals proteins involved in the progression from non-cancerous lesions to gastric cancer. Journal of Proteomics, 186:15–27. DOI: 10.1016/j.jprot.2018.07.013
Lecturas recomendadas
- Espino de la Fuente, C. (2018). Mitocondrias: más allá de la producción de energía celular. Cienciorama. http://www.cienciorama.unam.mx/#!titulo/555/?mitocondrias--mas-alla-de-la-produccion-de-energia-celular
- Méndez O. y Almazán A. (2018). Mitocondrias – El “ying-yang” de la vida. Recursos Naturales y Sociedad, 2018. Vol. 4 (1): 12-21. DOI: https://doi.org/10.18846/renaysoc.2018.04.04.01.0001
Comparte este artículo en redes sociales

Acerca de los autores
Dra. Diana Lashidua Fernández Coto; Investigadora Posdoctoral en el Laboratorio de Proteómica del CCG-UNAM. Q.F.B Marisol Ayala Reyes; estudiante de Maestría en Ciencias Bioquímicas en el Laboratorio de Proteómica del CCG-UNAM.
Contacto: dianafer@ccg.unam.mx; marisol.ayala@ibt.unam.mx